一、合同拟定
伦理审查通过后(以申办方获得伦理批件为准),申办方/CRO/SMO与PI及其研究团队共同拟定合同内容,形成合同初稿。
1.拟定主合同推荐使用我院提供的《临床试验合同模板》《检验检查费用价目表》(见下载专区),拟定CRC协议推荐使用我院提供的《临床试验CRC三方协议模板》(见下载专区)。
2.拟定过程中与PI确认费用、提供的设备、放置的场地等。检验检查费用除参考下载区的价目表外可联系机构办,机构办再与相关科室沟通确认。若对辅助科室有特殊的协助需求,提前向机构办提出,便于机构办联系辅助科室沟通协商。
二、合同审核
1.申办方/CRO/SMO将合同初稿(Word版,若使用医院模板有修改请发修改留痕版)发送至机构办邮箱(邮箱号:swyjgb2024@163.com,邮件标题格式:申办方简称-试验药品简称-试验分期-方案编号-主合同(临床试验合同)/补充合同/CRC协议),由机构办秘书初审,审核内容包括但不限于:双方的职责和义务、入组例数及期限、经费及经费支付方式(需附言项目名称和PI信息)、保险和赔偿、资料保存方式和年限、是否提供CRC或CRC费用、知识产权、成果分享、保密合同、仲裁条款(地点、语言、使用范围)等。
2.机构办秘书反馈初审意见给申办方/CRO/SMO,申办方/CRO/SMO根据反馈意见修改并经秘书最终审核通过后,再通过上传OA或纸质审核的形式,依次经主要研究者、专业科室负责人、财务、法务、机构办主任、机构主任审批会签,法务审核意见以法务所在的律师事务所出具的法律审核意见为准。
3.机构秘书将各级审核意见反馈给PI以及申办方/CR0/SMO,直至各审批部门审核同意。
4.合同最终审核完成会签。
三、合同签署
合同最终审核完成会签后,机构办主任/秘书将定稿后的合同发申办方/CRO/SMO指定邮箱,申办方/CRO/SMO法定代表人或授权代表签字、签日期并盖公章和骑缝章后交给主要研究者签字、签日期,主要研究者签字、签日期后递交给机构办审核,机构办审核通过后再递交给机构主任审批签字、签日期,最后再由机构办向医院办公室申请盖公章和骑缝章。
1.若合同为授权代表签字,则必须提供盖公司鲜章的授权书和盖公司鲜章的法人、授权代表的身份证复印件;若合同盖签字章,必须提供盖鲜章的授权书;若申办方/CR0/SMO公司盖合同专用章,需提供该合同专用章的公安局备案资料或出具盖有公章的合同章使用说明。合同首页和合同签署页都必须盖鲜章。
2.主合同后面签署的与该项目相关的其他合同都视为该主合同的补充合同。
3.合同签署后,机构办秘书联系财务科、信息科申请项目记账账号并为项目建项,同时联系申办方/CRO/SMO领取合同(一般为递交合同后5~10个工作日)以及准备项目启动事宜。
四、下载专区
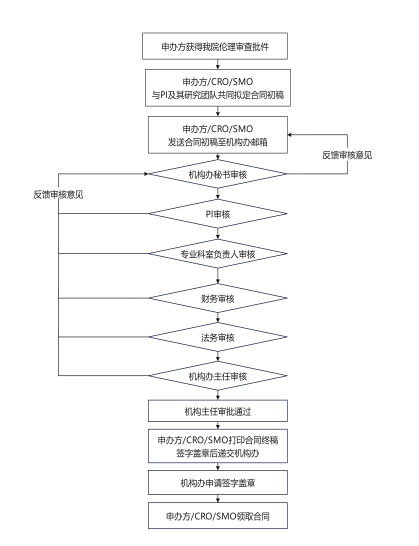
五、流程图